Генетические заболевания и борьба с ними
О настоящем и будущем лекарств на основе РНК-интерференции. В гостях у ведущего передачи «Вопрос науки» Алексея Семихатова кандидат химических наук Тимофей Сергеевич Зацепин.
Уже более 50 лет известны догмы молекулярной биологии: есть ДНК, из ДНК получается РНК, из РНК — белок. Белки определяют функции организма. Более того, чтобы соответствовать моменту, вам все время надо синтезировать новые белки и убирать старые. Вы вышли на солнце, вы ушли в тень, вы нырнули в воду, все охладилось, вам надо переварить обед — каждый раз вам необходимо синтезировать новые белки.
К сожалению, есть проблема, что при копировании ДНК иногда возникают ошибки. Существует колоссальный механизм для их исправления, но он справляется не всегда. Иногда это приводит к тому, что возникают белки, токсичные для организма. Генетические заболевания — это ситуация, когда в ДНК содержатся ошибки, приводящие к появлению белка, токсичного для организма. На разных этапах жизни у людей происходит синтез разных белков. Потому что у детей одна ситуация, у взрослых — другая. Пожилой возраст также иногда характеризуется другим набором белков.
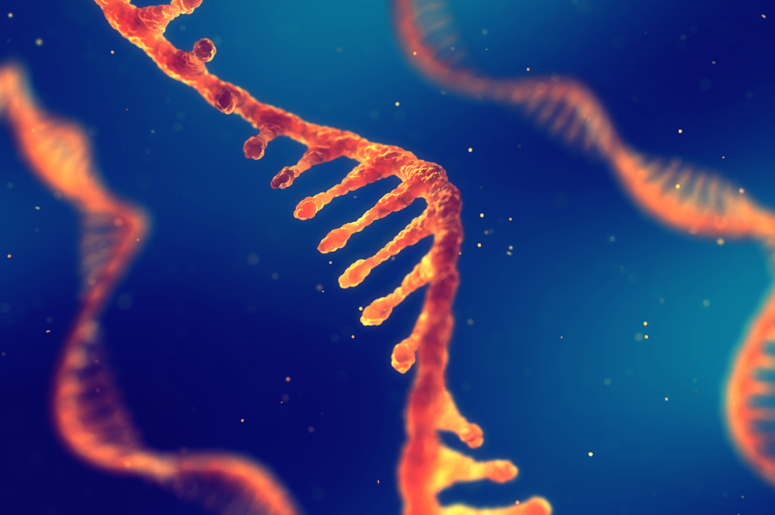
Любые сложные организмы устроены так, что РНК необходима. ДНК хранится в ядре, синтез белка происходит в цитоплазме — это два разных места в клетке. Необходимо передать информацию из одного места в другое. Как письмо. РНК-интерференция позволяет стереть письма с известным содержанием. То есть вы можете уничтожить все письма, в которых содержится определенное предложение. К сожалению, вы должны знать об этом заранее. В этом недостаток метода. Но если вы знаете и хотите уничтожить какую-то определенную РНК, это реализуется с помощью механизма РНК-интерференции.
Слово «интерференция» в данном случае означает «воздействие». Это природный механизм. Изначально клетка придумала его для борьбы с вирусами. Потому что, когда происходит заражение вирусами, в клетке одномоментно оказывается большое количество чужеродной ДНК и известные двухцепочечные РНК вирусов, и в этой ситуации включается механизм РНК-интерференции.
Клетка сначала нарезает чужеродную РНК на короткие фрагменты, а потом ищет РНК, которые комплементарны этим коротким фрагментам. И разрезает их. Замечательность метода заключается в том, что вы можете внести снаружи в клетку короткий фрагмент РНК, комплементарный любой интересующей вас мишени. И он будет работать по этому механизму.
Само явление было открыто в 1998 году, а компании, которые предполагали использовать это для терапии, были созданы уже в 2000–2001 годах, всего лишь через два-три года после открытия этого явления. Более того, это явление достаточно быстро получило признание, и в 2006 году за него была вручена Нобелевская премия.
Сначала люди пытались доставлять в клетку длинную двухцепочечную РНК, чтобы запустить этот механизм, потому что вирусы доставляют длинную РНК, — в надежде, что будет эффективное разрезание того, чему комплементарна эта длинная РНК. На самом деле сначала это пытались использовать в качестве инструмента для исследования, не для терапии. То есть вы можете таким образом убрать любую РНК, которая вам интересна, и посмотреть, к каким последствиям это приведет.
Длинная РНК оказалась плоха тем, что она вызывает сильный иммунный ответ, потому что у клетки существует много эшелонов борьбы с вирусными инфекциями, и РНК-интерференция — это не единственный инструмент. Также существует внутриклеточный иммунный ответ, который предназначен для борьбы с вирусами и который узнает такие длинные РНК.
Для ответа на лекарство, безусловно, это плохо, потому что иммунный ответ всегда провоцирует воспаление и другие неподходящие реакции. Поэтому придумали вводить короткие фрагменты, которые не узнаются внутриклеточными рецепторами и которые вызывают специфичную, именно РНК-интерференцию. Из-за того что в природе такие короткие фрагменты в клетку не попадают, она этому и не обучена, у нее нет механизма борьбы лично с ними. Но они запускают тот механизм, который нам в данном случае желателен.
«Патисиран», первый препарат, который одобрен американским FDA для медицинской практики, не содержит ни одного природного нуклеотида. Все они модифицированы. Белковый комплекс, который участвует в РНК-интерференции, его узнает, и все работает хорошо. А ферменты, которые разрезают РНК на части, не узнают его и разрезать не могут. Более того, сейчас препараты, которые находятся на второй и третьей стадии клинических испытаний, стабильны в организме до полугода. Вы видите эффект до восьми-девяти месяцев после однократного введения.
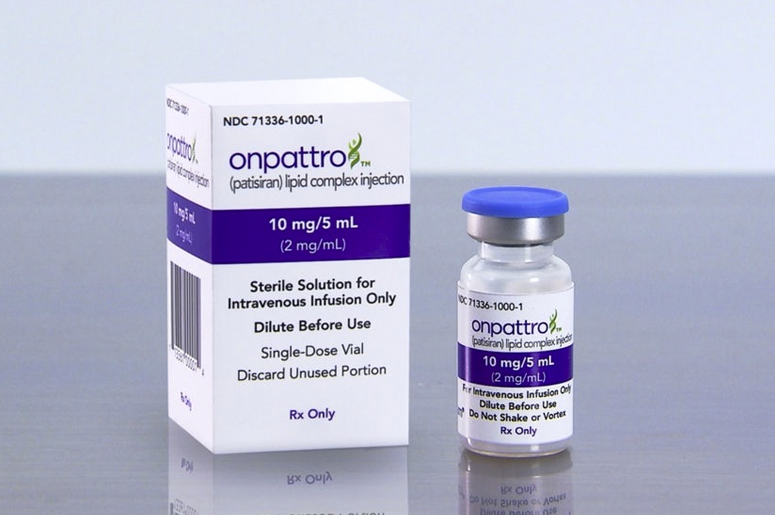
Лекарство необходимо доставлять не в каждую клетку организма, а в каждую клетку того органа, который экспрессирует неправильный белок. Это отдельная история — так называемая адресная доставка, которая представляет собой большую проблему и до конца она еще не решена. Проблема решена для печени. Но если вы захотите доставить лекарство в мышцы, или в мозг, или в какой-нибудь другой орган, это будет отдельная сложная история. Печень вообще является уникальным органом у человека. Она выполняет колоссальное количество функций, и многие из них связаны с тем, что она захватывает какие-то вещества, какие-то выбрасывает наружу. Поэтому на клеточной мембране есть специальные белки — так называемые клеточные рецепторы, которые узнают специфические молекулы. И таким образом, используя эти рецепторы, вы можете доставить лекарство именно в клетки печени РНК.
Молекулы РНК, или молекулы РНК, упакованные в какие-нибудь контейнеры, плавают везде. Но схватываются они только клетками печени. Рецепторы предназначены именно для этого. Они узнают молекулу и затаскивают ее внутрь клетки. Упаковка может быть разной: есть рецепторы, которые чувствительны к размеру, есть те, которые способны затащить практически любой контейнер. Многие клетки, которые что-то затаскивают снаружи, предназначены для того, чтобы это что-то разрушить. И тогда, как ни проводи химическую модификацию, это все равно приводит к разрушению РНК. В первую очередь это клетки иммунной системы. Есть проблемы гемато-энцефалического барьера. Просто сделав внутривенную инъекцию, контейнер никогда не сможет попасть в головной мозг, не пройдя этот барьер.
Расскажу, чем интересен и уникален этот класс лекарственных средств. До сих пор традиционный подход был основан на том, что использовались либо малые молекулы, либо антитела для того, чтобы блокировать белки. И в этой ситуации разработка препарата стоит достаточно дорого. Время составляет до десяти лет, стоимость может доходить до $1 млрд. Разработка, регистрация, вывод на рынок. Для РНК ситуация становится проще. Как только у вас есть средство доставки, которое позволяет эффективно доставлять препарат в определенный орган, то дальше вы можете относительно просто, быстро и дешево подобрать другую молекулу РНК, комплементарную другой мишени, и это может использоваться для терапии другого заболевания.
Это такой конструктор, то есть вы можете быстро сделать новый препарат. Его свойства будут сильно отличаться от предыдущего — это позволит быстро провести клинические испытания и сделать лекарственное средство.
Перспективы открываются в первую очередь для терапии так называемых редких, или орфанных, заболеваний. На сегодняшний день известно не менее 7000 заболеваний, когда ими на земном шаре страдает 10 000 человек и меньше. Для таких заболеваний невыгодно разрабатывать лекарственные средства. Поэтому менее чем для 500 из них известна терапия. Потому что, когда у вас есть 1000 больных на земном шаре, вы тратите $1 млрд на разработку препарата и после этого эти деньги никогда не сможете вернуть. Это просто невыгодно фарм-компаниям.
Для того чтобы решить эту проблему, можно использовать механизм РНК-интерференции. На сегодняшний день хорошо разработана доставка РНК в печень. С этим связана масса заболеваний. Вы можете, варьируя фрагменты РНК, быстро разрабатывать новые препараты. Собственно, это сейчас и происходит. Несмотря на то что сегодня зарегистрирован один препарат, не менее 50 из них находятся на разных стадиях клинических испытаний. Безусловно, не все из них дойдут до стадии лекарственного средства. Часть из них не получится. Но тем не менее будет решена проблема многих орфанных заболеваний.
Для меня более интересным является доставка в определенный тип клеток, или тканей, или органов. А также интересен поиск новых мишеней. На самом деле догма молекулярной биологии была предложена в конце 50-х годов, и с тех пор ситуация резко усложнилась. Было открыто колоссальное количество новых механизмов регуляции. И очень часто вы можете воздействовать не на РНК, кодирующую белок, а на другие регуляторные РНК. Некая цепочка событий в клетке все равно приведет к тому, что этот белок или не будет синтезироваться, или будет синтезироваться менее эффективно, или пойдет синтез какого-то альтернативного белка, который выполняет похожую функцию. Потому что сегодня РНК, кодирующая белок, составляет порядка 2–3% от всей РНК, которая синтезируется в клетке.
Таким образом, когда вы говорите про другие мишени, их может быть практически бесконечное количество, и многие из них связаны не только с наследственными заболеваниями, но и с развитием вирусных и онкологических заболеваний. Из тех 50 препаратов, про которые я говорил, не менее половины относятся к терапии онкологических заболеваний. Порядка 10% — к терапии вирусных заболеваний.



















