Дети с исправленными генами
Генетик и молекулярный биолог Денис Ребриков из Национального медицинского исследовательского центра акушерства, гинекологии и перинатологии имени В. И. Кулакова объявил о готовности заняться «починкой» наследственной глухоты при помощи генной модификации эмбрионов человека. Технология уже опробована на модельных животных и клетках человека, найдены пять семейных пар, которые хотели бы поучаствовать в этом опыте. В настоящий момент ученый ждет одобрения государственных регуляторов — решение будет принимать Этический комитет Минздрава РФ и Департамент лекарственного обеспечения и регулирования обращения медицинских изделий. Пока планы российского биолога активно обсуждаются в мировых СМИ, мы решили побеседовать с ним самим — о технологии, ее применении и будущем генной инженерии.
Денис Владимирович, расскажите, пожалуйста, о какой технологии идет речь? И как она будет применяться в медицине?
Около пяти лет назад ученые в лабораториях стали использовать принципиально новый подход к внесению направленных изменений в ДНК. Этот подход получил название «геномное редактирование, основанное на CRISPR/Cas». Почему эта технология вызвала такой ажиотаж даже тогда, когда это были чисто научные эксперименты? Потому что она существенно упростила саму методику внесения изменений. До этого ученые тоже умели менять последовательность ДНК, но методика была гораздо сложнее в исполнении. Здесь произошел переход качества в количество, то есть появился новый удобный молекулярный инструмент и это сразу породило гигантское количество научных исследований, в рамках которых ученые, используя генетический редактор CRISPR/Cas, стали вносить изменения в разные геномы модельных объектов: животных, бактерий, растений. Если вы посмотрите базу научных статей за последние пять лет, там уже больше 15 000 научных работ, основанных на методе внесения изменений в геном с помощью CRISPR/Cas. И самих CRISPR/Cas на сегодняшний день уже изобретено десятки разных вариантов.
Естественно, что исследователи стали смотреть, можно ли применить эту технологию в медицине. И здесь возможны два направления. Первое — это соматическое генное редактирование: когда человек уже живет и оказывается, что у него есть патогенные мутации. Эти мутации, в свою очередь, бывают двух типов. Во-первых, это наследственные моногенные заболевания: например, дистрофия Дюшенна, муковисцидоз, наследственная тугоухость и еще более 7000 синдромов! Примерно каждый сотый ребенок рождается с мутациями, унаследованными от родителей и приводящими к тяжелым генетическим заболеваниям. Во-вторых, это так называемые соматические мутации: нарушения ДНК, не полученные от родителей, а возникшие в течение жизни. Они вызывают совсем другой спектр заболеваний — например, рак.
Соматическое редактирование — не новая терапия, ее используют уже десятки лет, но до настоящего момента она делалась не на CRISPR/Cas, а другими способами: доставкой целого гена при помощи вирусной конструкции. К сожалению, на данный момент во всем организме мы починить гены не можем, это возможно лишь в некоторых частях организма. В ряде случаев мы достаем клетки из пациента, чиним в них мутацию в лабораторных условиях и возвращаем клетки обратно человеку. Генное редактирование для борьбы с раком также применяется. Мы можем чинить поломанные гены в опухоли, и тогда клетки будут самоликвидироваться. Но это не мое направление, здесь я небольшой специалист.
Другое глобальное направление использования геномного редактирования — фетальное, когда мы делаем изменения в геноме на уровне единственной и самой первой клетки, из которой разовьется целый организм: зиготы. Эта технология довольно хорошо на сегодняшний день отработана на модельных животных: мышах, крысах, кроликах. На наших лабораторных животных мы умеем вносить изменения в первую клетку с тем, чтобы весь организм получился с измененной ДНК. Так исследователи изучают живые системы, внося разные изменения в геном и наблюдая, что меняется в программе развития организма. Этим занимается весь мир, выходят тысячи статей о геномном редактировании.
Чтобы понять, как устроена программа построения сверхсложной живой системы, надо что-то поменять в исходном коде. Это напоминает программирование. Программист пишет программу, а чтобы понять правильность кода, он ее запускает и смотрит, что получилось. Потом меняет код и снова запускает, оценивая работу. Генетики делают то же самое, но в обратную сторону. Мы не пишем генетический код, его уже написала эволюция, а наша задача — расшифровать программу, понять язык этого программирования и в конечном счете научиться корректировать программу. Для этого мы вносим изменения в код и запускаем его реализацию через рост живого организма. На животных, на одной клетке мы умеем все это делать. Возникает вопрос: актуально ли это в медицине? Чинить гены на стадии одной клетки до того, как организм начал развиваться?
Да, расскажите, пожалуйста! Это как раз самое интересное.
На самом деле таких случаев крайне мало. Оказалось, что актуальных случаев для применения геномного редактирования на уровне зиготы в медицине мало и по числу, и по видам заболеваний. Какие это случаи? Первый — это случай, который у всех на слуху: ВИЧ-инфицированные пациенты с множественной лекарственной резистентностью (устойчивостью). Это пациенты, не реагирующие на лечение (антиретровирусную терапию), у них в крови постоянно присутствует вирус. Если это женщина и если она планирует рождение ребенка, риск передачи вируса ребенку у нее во много раз выше, чем для обычных ВИЧ-положительных женщин. Сравните: для ВИЧ-положительной женщины с нормальным ответом на терапию риск передать вирус ребенку примерно 0,5%. То есть на 200 детей от ВИЧ-положительных матерей вирус передастся лишь одному новорожденному. Но если женщина ВИЧ-положительна, она плохо отвечает на противовирусную терапию и при этом хочет завести ребенка (смотрите, сколько «если»!), то один из возможных способов обеспечить рождение здорового ребенка — это сделать его генетически устойчивым к вирусу. Таких женщин по нашим расчетам крайне мало — 10–20 пациенток на всю Россию.
Как раз это и проделал недавно китайский ученый Хэ Цзянькуй, отредактировавший гены близнецов втайне от всех. Почему же это так возмутило научное сообщество?
Китайский исследователь действительно отредактировал геном будущих детей на уровне зиготы, но он использовал методику в неадекватной клинической ситуации: он неправильно выбрал пациентов. В его случае отец детей был ВИЧ-положительным, а мать — ВИЧ-отрицательной. Он неоправданно использовал геномное редактирование, поскольку для ВИЧ-инфицированного мужчины сегодня вообще нет проблемы родить ВИЧ-отрицательного ребенка: есть технология ЭКО с отмывкой сперматозоидов, после ее применения ребенок 100% рождается без ВИЧ. Китайского ученого все осудили не потому, что он что-то плохо сделал в плане технологий, нет — просто он взял неадекватный клинический случай. Зачем сверхновую, еще не проверенную технологию применять на людях, когда это не оправданно? Так делать нельзя, и я согласен с развернувшейся критикой. Технология для медицины должна быть либо очень хорошо проверенная, либо применяться в случаях, когда есть уникальный позитивный эффект от применения, которого невозможно достичь без новой технологии.
В каких еще случаях применение этой технологии оправданно?
Кроме примера с ВИЧ, о котором я уже рассказал, все остальные случаи — это случаи наследственных заболеваний, при которых все дети для данной пары родителей точно будут больными (и таких семей тоже очень-очень мало!). Как я уже упоминал выше, генетически больной ребенок рождается примерно в каждой сотой семье, но даже в этой семье вероятность рождения такого ребенка у родителей не 100%, обычно либо 25% либо 50% в зависимости от того, рецессивное это заболевание или доминантное.
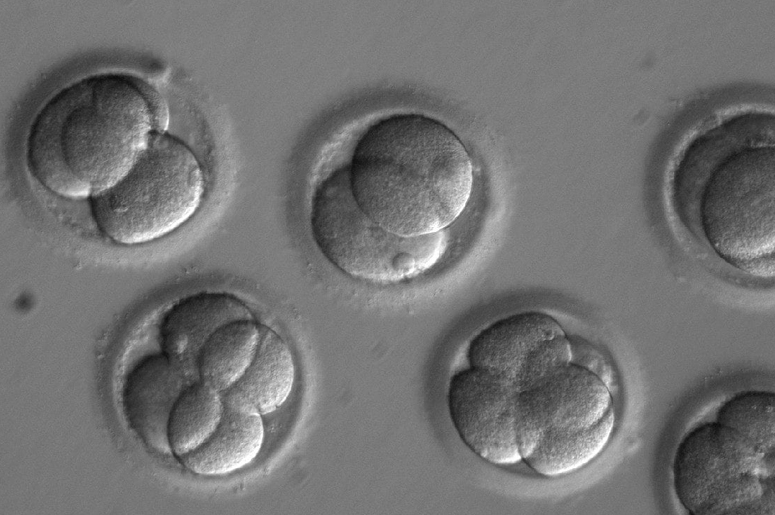
Представьте: живет пара абсолютно здоровых людей. И к сожалению, они про свою ДНК ничего не знают (несмотря на то, что на календаре уже 2019 год!). Рождается ребенок, и оказывается, что он болен: у него моногенное заболевание — например, муковисцидоз. Как же так вышло? Это следствие того, что у каждого из родителей была мутация, но она была только в одной хромосоме (у человека всех хромосом по две штуки), а вторая хромосома была здоровая. И поэтому человек был здоров (так называемый носитель мутации), а вот ребенок получился больным — с двумя поломанными хромосомами. Нужно ли таким людям геномное редактирование эмбрионов? Нет! Они могут пойти на обычное ЭКО, и мы выберем генетически здоровый эмбрион путем тестирования на стадии всего 250 клеток! Никакого редактирования генома не требуется.
Очень важно донести до читателей понимание этого момента. Чтобы избежать рождения тяжело больного ребенка с наследственным моногенным заболеванием, никакого геномного редактирования не требуется. В 99,9% случаев достаточно преимплантационного генетического тестирования эмбрионов перед переносом в матку. Единственное важное условие: необходимо заранее знать, что у этой пары будущих родителей есть риск рождения больного ребенка, после этого они идут на ЭКО и мы отбираем им здоровый эмбрион. К сожалению, мы узнаем об этих рисках лишь после того, как у пары родился первый больной ребенок.
А возможно ли заранее узнать риски рождения больного ребенка?
Можно. Но на сегодня эта процедура — определение полной последовательности генома или хотя бы его смысловой части, экзома, — довольно дорогостоящая (от 30 000 руб.). Потому это не массовое явление. Если мы перенесемся в не очень далекое будущее — лет на десять вперед, все люди в медкарте будут иметь свой геном. Тогда мы будем знать заранее, что у этой конкретной пары потенциальных родителей есть риск рождения ребенка с наследственным заболеванием, поэтому их надо сразу отправлять на ЭКО. В мире уже есть страны, где правительство приняло решение всех генотипировать и использовать эти данные, в том числе для профилактики рождения детей с тяжелыми заболеваниями.
Когда все-таки уместно применять геномное редактирование?
Как я уже сказал, случаев оправданного применения геномного редактирования на уровне зиготы очень мало, поскольку оба родителя должны быть мутантны по обеим хромосомам каждый (то есть быть больны аутосомно-рецессивным заболеванием). Это крайне редкие ситуации, потому, что, несмотря на 7000 известных нам моногенных наследственных заболеваний, каждое из них крайне редко и вероятность образования такой семьи очень мала. Но есть примеры «стремления» таких людей друг у другу. Например, наследственная тугоухость. Глухие образуют семьи внутри своего сообщества, ведь они общаются на одном языке. Оказалось, что наследственная тугоухость связана с нарушением одного и того же белка — это коннексин 26 (ген GJB2) в 80% случаев. В трети из них речь идет об одной и той же мутации. На сегодня в России живут десятки семей, где оба супруга глухие с одним и тем же нарушением и у них зачастую уже родился первый глухой ребенок. И в данном случае мы заранее знаем, что все их дети будут генетически глухими (правда, сегодня есть достаточно эффективный способ реабилитации — кохлеарная имплантация, позволяющая таким детям слышать). Это пример, когда без исправления мутации на стадии первой клетки мы ни при каких отборах на ЭКО не можем получить ребенка с нормальным слухом. Здесь только исправление мутации на стадии зиготы.
Есть еще некоторые более редкие случаи. Похожая история с дварфизмом (карликовостью). Люди одинакового фенотипа образуют семьи, но эта ситуация гетерогенна: люди имеют такой фенотип из-за очень разных генетических причин. Хотя встречаются и пары с совпадающими мутациями, у них и дети рождаются такие же.

Почему некоторые ваши коллеги считают, что «чинить» эмбрионы при таких болезнях неэтично?
Да, это очень сложный вопрос… Недавно меня удивило рассуждение одного англоязычного издания примерно следующего содержания: «Кто вообще сказал, что глухота — это заболевание? Или карликовость? Это просто люди с такой особенностью. Кто вообще дает ученым право предлагать этим людям исправлять эти нарушения ДНК с тем, чтобы у них рождались дети с обычным фенотипом? Может быть, им комфортно в их социальной группе?» Мол, это их ниша, они так живут, у них все хорошо и дети пусть у них рождаются без слуха или с низким ростом. Западное общество гипертрофированно корректно. Я отчасти соглашусь, говоря про дварфизм. Действительно, люди с таким фенотипом нормально живут и они точно могут самореализоваться. Есть примеры, когда они становятся звездами в Голливуде и на телеэкране. И говорить, что такой фенотип надо непременно исправлять для их детей, пожалуй, некорректно.
Но с глухотой другая ситуация. Это инвалидность. Людей с отсутствием слуха (и даже с кохлеарным имплантатом) не во все профессии возьмут. Есть масса ограничений в социуме, которые коснутся ребенка с глухотой. К сожалению, глухие родители даже не всегда согласны реабилитировать родившегося глухого ребенка, то есть ставить ему кохлеарный имплантат, который позволит ему слышать. Бывают категорические отказы делать эту операцию. Это сложно понять, но можно предположить, что они не видят целесообразности этой операции, потому что общаются с ребенком на языке жестов и не смогут общаться с ним голосом. Если они сделают операцию, ребенок будет больше общаться с внешним миром, а не с ними. С другой стороны, возможно, они опасаются и самого хирургического вмешательства, ведь это надо внутрь головы вживлять имплантат. Боятся операции и осложнений, говорят: «Не надо. Мы живем, и он проживет».
Генетики же могут предложить такой семье другой выход: ребенок сразу родится с нормальным геном коннексина, без всяких операций. Слышащий ребенок будет лучше развиваться — недаром реабилитологи настаивают, чтобы всем глухим детям устанавливали имплантаты.
На сегодняшний день технология геноредактирования на уровне зиготы не допущена к медицинскому применению по двум причинам: во-первых, почти нет клинически оправданных случаев, а во-вторых, потому что не доказана ее безопасность. Так вот, у нас есть возможность доказать это корректно. Сейчас мы доказываем для случаев ВИЧ и глухоты, что применение эффективно и безопасно, и надеемся получить разрешение наших регуляторов для того, чтобы применить это для клинически оправданных случаев.
Как вам кажется, каково будущее такого рода экспериментов?
Первые несколько десятков, возможно, сотен случаев применения геномного редактирования на уровне зиготы по всему миру должны быть однозначными с точки зрения клинической оправданности. Это должны быть случаи, понятные общественности: «Благодаря новой медицинской технологии родился здоровый ребенок». И только после того, как это будет применено многократно в разных точках планеты разными врачами и будут получены хорошие результаты, следующим большим блоком применения станет исправление мутаций, которые приводят к развитию заболеваний у людей во взрослом состоянии. Мы сможем «заранее» чинить предрасположенность к развитию заболевания, то есть мутации, вызывающие раннее развитие инсульта, инфаркта, нейродегенеративных заболеваний.
Дело в том, что многие заболевания бывают в хронической форме и агрессивной. Когда мы говорим о развитии, например, пародонтита в пожилом возрасте — это нормально, мы ничего с этим не можем поделать. Но бывают формы агрессивного пародонтита, когда у человека в 30 лет зубы выпадают. Это как раз генетика. Такого человека надо было бы «починить». Состояние совместимо с жизнью? Да. Но хорошо ли, если у всех детей в данной семье зубы начнут выпадать в 30 лет? Но это будет уже следующий шаг, и таких случаев гораздо больше, чем те, которыми мы сейчас занимаемся.
Научное сообщество очень переживает по поводу редактирования генов. Это переживания и об этичности, и о рисках. Какова вероятность, что что-то пойдет не так?
В любом медицинском вмешательстве есть риски. Когда вы покупаете таблетки, в инструкции написано: возможна индивидуальная непереносимость препарата. Какое-то количество людей на планете умирают из-за того, что съели аспирин. Абсолютно безрисковых препаратов не бывает. Мы будем стремиться к тому, чтобы безопасность срабатывания этой системы CRISPR/Cas была адекватна той пользе, которую получает в результате человек.
|
|
Генетик и молекулярный биолог Денис Ребриков из Национального медицинского исследовательского центра акушерства, гинекологии и перинатологии имени В. И. Кулакова |























