Выращенный в лаборатории мозг научился играть в понг

Австралийская компания Cortical Labs совершила прорыв в изучении неврологических заболеваний. Их система синтетического биологического интеллекта (SBI), основанная на выращенных в лаборатории человеческих нейронах, впервые продемонстрировала способность обучаться в реальном времени под действием противосудорожных препаратов. Исследование, опубликованное в журнале Communications Biology, показало, как нейроны, моделирующие эпилепсию, изменяют свою активность и улучшают выполнение задач в игровой среде после медикаментозного воздействия.
Важная веха для медицины и науки
Эпилепсия — одно из самых распространенных неврологических заболеваний, при котором в мозге происходят неконтролируемые всплески электрической активности, вызывающие судороги. У 30 % пациентов традиционные препараты оказываются неэффективными. При этом исследования часто проводятся на животных, чья мозговая деятельность существенно отличается от человеческой, что снижает точность и эффективность терапии.
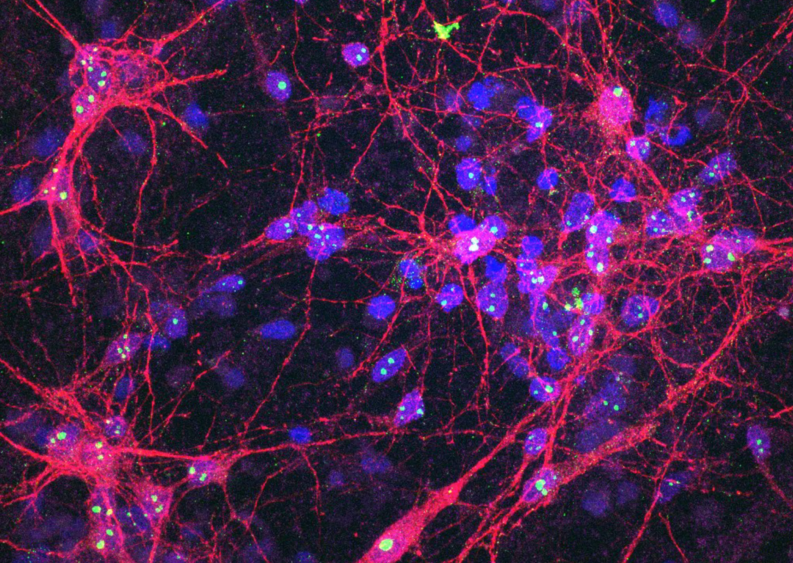
Платформа SBI меняет подход: она использует нейроны, выращенные из индуцированных плюрипотентных стволовых клеток человека (hiPSC). Эти клетки способны превращаться в любые типы клеток организма. Поместив нейроны на кремниевую платформу, ученые получили нейросети, которые могут воспринимать сигналы и отвечать на них в реальном времени, имитируя поведение мозга.
Система, получившая название DishBrain, содержит около 800 000 нейронов человека и мыши, выращенных в лаборатории. Они размещены на массиве электродов, соединенных с компьютером, который запускает упрощенную версию игры Pong — виртуального пинг-понга. Нейроны получают электрические сигналы (например, координаты мяча) и в ответ активизируются, обучаясь через процесс нейропластичности — естественную способность мозга формировать новые связи.
В рамках эксперимента в нейронах искусственно вызвали состояние, похожее на эпилепсию. Для этого применили метод глутаматергической дисрегуляции — нарушения баланса возбуждающего нейромедиатора глутамата, приводящего к чрезмерной активности нейронов.
После 21 дня дифференциации (процесса превращения стволовых клеток в нейроны) команда протестировала три противосудорожных препарата: дифенин, перампанель и карбамазепин. Последний, в дозе 200 мкМ ≈ 47,3 мкг/мл, оказался самым эффективным — он не только уменьшил чрезмерную активность, но и улучшил поведение нейросети, сделав ее более стабильной и организованной во время игры. В клинической практике карбамазепин назначается обычно в дозах 200–1200 мг в сутки в виде таблеток.
Ключевые результаты
-
Все три препарата снижали эпилептическую активность, но только карбамазепин усиливал обучаемость нейросети.
-
Нейронные связи стали более упорядоченными, что отражает рост способности к саморегуляции.
-
SBI позволяет одновременно тестировать разные препараты на моделях нейронных расстройств, что ускоряет разработку новых методов терапии.
«Способность наблюдать, как живые нейроны реагируют на стимуляцию и медикаментозное лечение в реальном времени, открывает новые способы разработки и персонализации лечения», — подчеркивает Бретт Каган, главный научный сотрудник лаборатории
Важно то, что можно мгновенно отслеживать реакцию клеток на лекарства, а нейроны можно выращивать из клеток конкретного пациента, подбирая индивидуальное лечение.
Платформа пока моделирует только часть мозга, фокусируясь на глутаматергических нейронах, но это уже серьезный шаг вперед.
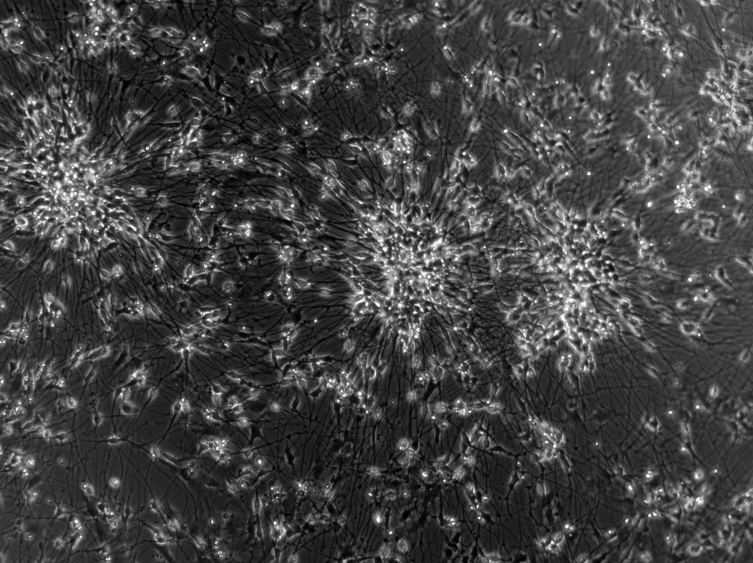
«Мы показываем, что нейронные функциональные параметры могут быть улучшены с помощью лекарственного вмешательства — это открывает дверь к более значимым критериям эффективности в терапии», — говорит Брэд Ватмуфф, руководитель отдела биологии Cortical Labs.
Компания уже работает над расширением платформы CL1, чтобы использовать ее для моделирования болезни Альцгеймера, аутизма и других сложных нарушений мозга. Это может радикально повысить эффективность клинических испытаний, ведь сегодня до 90 % препаратов от неврологических болезней проваливаются из-за сложности мозга и неадекватности моделей.


































